| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Cesium-137: Cesium-137 , eller radiokasium , er en radioaktiv isotop av cesium som dannes som et av de mer vanlige fisjonproduktene av atomfisjonen av uran-235 og andre spaltbare isotoper i atomreaktorer og atomvåpen. Spormengder stammer også fra naturlig fisjon av uran-238. Det er blant de mest problematiske av fisjonproduktene med kort til middels levetid. Når den plutselig slippes ut ved høy temperatur, som i tilfellet med atomulykken i Tsjernobyl og med atombombeeksplosjoner, på grunn av elementets relativt lave kokepunkt, blir 137 C lett fordampet i atmosfæren og transportert i luften på svært lange avstander . Etter det radioaktive nedfallet avsettes det på jorden og beveger seg lett og sprer seg i miljøet på grunn av den høye vannløseligheten til caesiums vanligste kjemiske forbindelser, som er salter. 137 Cs ble oppdaget av Glenn T. Seaborg og Margaret Melhase. |  |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Isotoper av cesium: Cesium ( 55 Cs) har 40 kjente isotoper, noe som gjør det, sammen med barium og kvikksølv, til et av elementene med flest isotoper. Atommassene til disse isotopene varierer fra 112 til 151. Bare en isotop, 133 Cs, er stabil. Radioisotopene med lengst levetid er 135 Cs med en halveringstid på 2,3 millioner år, 137 Cs med en halveringstid på 30,1671 år og 134 Cs med en halveringstid på 2,0652 år. Alle andre isotoper har halveringstider mindre enn 2 uker, de fleste under en time. | |
| Cesium-137: Cesium-137 , eller radiokasium , er en radioaktiv isotop av cesium som dannes som et av de mer vanlige fisjonproduktene av atomfisjonen av uran-235 og andre spaltbare isotoper i atomreaktorer og atomvåpen. Spormengder stammer også fra naturlig fisjon av uran-238. Det er blant de mest problematiske av fisjonproduktene med kort til middels levetid. Når den plutselig slippes ut ved høy temperatur, som i tilfellet med atomulykken i Tsjernobyl og med atombombeeksplosjoner, på grunn av elementets relativt lave kokepunkt, blir 137 C lett fordampet i atmosfæren og transportert i luften på svært lange avstander . Etter det radioaktive nedfallet avsettes det på jorden og beveger seg lett og sprer seg i miljøet på grunn av den høye vannløseligheten til caesiums vanligste kjemiske forbindelser, som er salter. 137 Cs ble oppdaget av Glenn T. Seaborg og Margaret Melhase. |  |
| Cesium-137: Cesium-137 , eller radiokasium , er en radioaktiv isotop av cesium som dannes som et av de mer vanlige fisjonproduktene av atomfisjonen av uran-235 og andre spaltbare isotoper i atomreaktorer og atomvåpen. Spormengder stammer også fra naturlig fisjon av uran-238. Det er blant de mest problematiske av fisjonproduktene med kort til middels levetid. Når den plutselig slippes ut ved høy temperatur, som i tilfellet med atomulykken i Tsjernobyl og med atombombeeksplosjoner, på grunn av elementets relativt lave kokepunkt, blir 137 C lett fordampet i atmosfæren og transportert i luften på svært lange avstander . Etter det radioaktive nedfallet avsettes det på jorden og beveger seg lett og sprer seg i miljøet på grunn av den høye vannløseligheten til caesiums vanligste kjemiske forbindelser, som er salter. 137 Cs ble oppdaget av Glenn T. Seaborg og Margaret Melhase. |  |
| Cesium kadmiumbromid: Cesium kadmiumbromid (CsCdBr 3 ) er et syntetisk krystallinsk materiale. Det tilhører AMX 3 -gruppen (hvor A = alkalimetall, M = bivalent metall, X = halogenion). I motsetning til de fleste andre bromider er CsCdBr 3 ikke-hygroskopisk, noe som gir den applikasjoner som et effektivt oppkonverteringsmateriale i solceller. Som en enkelt krystallstruktur dopet med sjeldne jordarter, kan den også brukes som aktivt lasermedium. Det er svært gjennomsiktig i de synlige og infrarøde områdene og kan brukes som et ikke -lineært optisk krystall. |  |
| Cesiumkarbonat: Cesiumkarbonat eller cesiumkarbonat er en hvit krystallinsk fast forbindelse. Cesiumkarbonat har høy oppløselighet i polare løsningsmidler som vann, alkohol og DMF. Løseligheten er høyere i organiske løsningsmidler sammenlignet med andre karbonater som kalium og natriumkarbonater, selv om den forblir ganske uløselig i andre organiske løsningsmidler som toluen, p-xylen og klorbenzen. Denne forbindelsen brukes i organisk syntese som en base. Det ser også ut til å ha applikasjoner innen energikonvertering. | 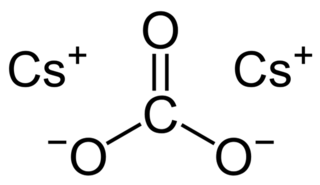 |
| Cesiumfluorid: Cesiumfluorid eller cesiumfluorid er en uorganisk forbindelse med formelen CsF og er et hygroskopisk hvitt salt. Cesiumfluorid kan brukes i organisk syntese som en kilde til fluorid -anionen. Cesium har også den høyeste elektropositiviteten til alle ikke-radioaktive elementer, og fluor har den høyeste elektronegativiteten av alle elementene. |  |
| Cesiumacetat: Cesiumacetat eller cesiumacetat er en ionisk cesiumforbindelse med molekylformelen CH 3 CO 2 Cs. Det er et hvitt fast stoff som kan dannes ved reaksjon av cesiumhydroksyd eller cesiumkarbonat med eddiksyre. |  |
| Cesiumstandard: Cesiumstandarden er en primærfrekvensstandard der fotonabsorpsjonen ved overganger mellom de to hyperfine jordtilstandene til cesium-133 atomer brukes til å kontrollere utgangsfrekvensen. Den første cesiumklokken ble bygget av Louis Essen i 1955 ved National Physical Laboratory i Storbritannia. og promotert over hele verden av Gernot MR Winkler fra United States Naval Observatory. |  |
| Cesium aurid: Cesiumurid er den uorganiske forbindelsen med formelen CsAu. Det er Cs + salt av uvanlig Au - anion. |  |
| Cesiumazid: Cesiumazid eller cesiumazid er en uorganisk forbindelse av cesium og azid med formelen CsN |  |
| Cesiumbikarbonat: Cesiumbikarbonat eller cesiumbikarbonat er en kjemisk forbindelse med den kjemiske formelen CsHCO 3 . Det kan produseres gjennom følgende reaksjon:
|  |
| Cesium bisulfat: Cesium bisulfat eller cesium-hydrogensulfat er en uorganisk forbindelse med formelen CsHSO 4. Cesiumsaltet av bisulfat, det er et fargeløst fast stoff oppnådd ved å kombinere Cs 2 SO 4 og H 2 SO 4 . |  |
| Cesiumbromid: Cesiumbromid eller cesiumbromid er en ionisk forbindelse av cesium og brom med den kjemiske formelen CsBr. Det er et hvitt eller gjennomsiktig fast stoff med smeltepunkt ved 636 ° C som lett oppløses i vann. Massekrystallene har den kubiske CsCl-strukturen, men strukturen endres til steinsalttypen i nanometertynn film vokst på glimmer, LiF, KBr eller NaCl-underlag. |  |
| Cesium kadmiumbromid: Cesium kadmiumbromid (CsCdBr 3 ) er et syntetisk krystallinsk materiale. Det tilhører AMX 3 -gruppen (hvor A = alkalimetall, M = bivalent metall, X = halogenion). I motsetning til de fleste andre bromider er CsCdBr 3 ikke-hygroskopisk, noe som gir den applikasjoner som et effektivt oppkonverteringsmateriale i solceller. Som en enkelt krystallstruktur dopet med sjeldne jordarter, kan den også brukes som aktivt lasermedium. Det er svært gjennomsiktig i de synlige og infrarøde områdene og kan brukes som et ikke -lineært optisk krystall. |  |
| Cesium kadmiumklorid: Cesium kadmiumklorid (CsCdCl 3 ) er et syntetisk krystallinsk materiale. Det tilhører AMX 3 -gruppen (hvor A = alkalimetall, M = bivalent metall, X = halogenioner). Den krystalliserer seg i en sekskantet romgruppe P6 3 / mmc med enhetscellelengder a = 7.403 Å og c = 18.406 Å, med en kadmiumion med D 3d symmetri og den andre med C 3v symmetri. | |
| Cesiumkarbonat: Cesiumkarbonat eller cesiumkarbonat er en hvit krystallinsk fast forbindelse. Cesiumkarbonat har høy oppløselighet i polare løsningsmidler som vann, alkohol og DMF. Løseligheten er høyere i organiske løsningsmidler sammenlignet med andre karbonater som kalium og natriumkarbonater, selv om den forblir ganske uløselig i andre organiske løsningsmidler som toluen, p-xylen og klorbenzen. Denne forbindelsen brukes i organisk syntese som en base. Det ser også ut til å ha applikasjoner innen energikonvertering. |  |
| Cesiumklorid: Cesiumklorid eller cesiumklorid er den uorganiske forbindelsen med formelen CsCl. Dette fargeløse saltet er en viktig kilde til cesiumioner i en rekke nisjeapplikasjoner. Krystallstrukturen danner en hovedkonstruksjonstype hvor hvert cesiumion er koordinert av 8 klorioner. Cesiumklorid oppløses i vann. CsCl endres til NaCl -struktur ved oppvarming. Cesiumklorid forekommer naturlig som urenheter i karnallitt, sylvitt og kainitt. Mindre enn 20 tonn CsCl produseres årlig over hele verden, hovedsakelig fra et cesiumholdig mineralsk pollucitt. |  |
| Cesium kromat: Cesium kromat eller cesium kromat er en uorganisk forbindelse med formel Cs 2 CrO 4. Det er et gult krystallinsk fast stoff som er cesiumsaltet av kromsyre, og det krystalliserer i det orthorhombiske systemet. |  |
| Cesiumstandard: Cesiumstandarden er en primærfrekvensstandard der fotonabsorpsjonen ved overganger mellom de to hyperfine jordtilstandene til cesium-133 atomer brukes til å kontrollere utgangsfrekvensen. Den første cesiumklokken ble bygget av Louis Essen i 1955 ved National Physical Laboratory i Storbritannia. og promotert over hele verden av Gernot MR Winkler fra United States Naval Observatory. |  |
| Cesiumcyanid: Cesiumcyanid er cesiumsaltet av hydrogencyanid. Det er et hvitt fast stoff, lett oppløselig i vann, med en lukt som minner om bitre mandler, og med krystaller som ligner sukker. Cesiumcyanid har kjemiske egenskaper som ligner kaliumcyanid og er veldig giftig. | |
| Cesium dodecaborate: Cesium dodecaborate er en uorganisk forbindelse med formelen Cs 2 B 12 H 12 . Det er et salt, med cesiumkationer og [B 12 H 12 ] 2− anioner. Denne anionen har vært av stor teoretisk interesse for kjemisamfunnet. | 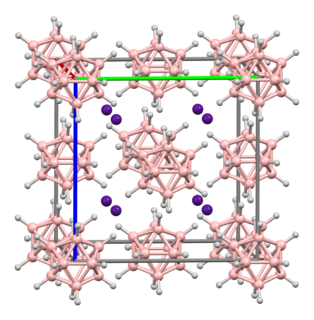 |
| Cesiumfluorid: Cesiumfluorid eller cesiumfluorid er en uorganisk forbindelse med formelen CsF og er et hygroskopisk hvitt salt. Cesiumfluorid kan brukes i organisk syntese som en kilde til fluorid -anionen. Cesium har også den høyeste elektropositiviteten til alle ikke-radioaktive elementer, og fluor har den høyeste elektronegativiteten av alle elementene. |  |
| Cesiumfluorid: Cesiumfluorid eller cesiumfluorid er en uorganisk forbindelse med formelen CsF og er et hygroskopisk hvitt salt. Cesiumfluorid kan brukes i organisk syntese som en kilde til fluorid -anionen. Cesium har også den høyeste elektropositiviteten til alle ikke-radioaktive elementer, og fluor har den høyeste elektronegativiteten av alle elementene. |  |
| Formater: Formiat er anionen avledet Et formiat (forbindelse) er et salt eller en ester av maursyre. | 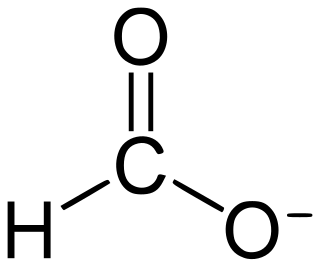 |
| Atomfontene: En atomfontene er en sky av atomer som kastes oppover i jordens gravitasjonsfelt av lasere. Hvis det var synlig, ville det ligne vannet i en fontene. Mens de er vektløse i kastet, måles atomene for å stille frekvensen til en atomur. |  |
| Tysk: Germane er den kjemiske forbindelsen med formel Ge H 4, og den germanium analog metan. Det er det enkleste germaniumhydrid og en av de mest nyttige forbindelsene av germanium. Som de beslektede forbindelsene silan og metan, er tysk tetraedrisk. Det brenner i luft for å produsere GeO 2 og vann. Germane er en gruppe 14 -hydrid. |  |
| Cesiumheksafluorokobaltat (IV): Cesiumheksafluorokobaltat (IV) er et salt med den kjemiske formelen Cs |  |
| Cesiumheksafluorokuprat (IV): Cesiumheksafluorokuprat er den uorganiske forbindelsen med den kjemiske formelen Cs
| 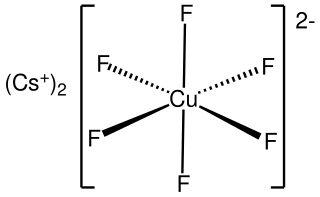 |
| Cesiumheksafluorokuprat (IV): Cesiumheksafluorokuprat er den uorganiske forbindelsen med den kjemiske formelen Cs
|  |
| Cesiumhydrid: Cesium hydrid eller cesium hydrid (CSH) er en forbindelse av cesium og hydrogen. Det er et alkalimetallhydrid. Det var det første stoffet som ble dannet av lysindusert partikkeldannelse i metaldamp, og viste løfte i tidlige studier av et ionfremdriftssystem som bruker cesium. Det er det mest reaktive stabile alkaliske metallhydridet av alle. Det er en kraftig superbase og reagerer ekstremt kraftig med vann. |  |
| Cesiumbikarbonat: Cesiumbikarbonat eller cesiumbikarbonat er en kjemisk forbindelse med den kjemiske formelen CsHCO 3 . Det kan produseres gjennom følgende reaksjon:
|  |
| Cesium bisulfat: Cesium bisulfat eller cesium-hydrogensulfat er en uorganisk forbindelse med formelen CsHSO 4. Cesiumsaltet av bisulfat, det er et fargeløst fast stoff oppnådd ved å kombinere Cs 2 SO 4 og H 2 SO 4 . |  |
| Cesiumhydroksid: Cesiumhydroksyd eller cesiumhydroksyd (CsOH) er en kjemisk forbindelse bestående av cesiumioner og hydroksidioner. Det er en sterk base (pK b = -1,76), omtrent som de andre alkalimetallhydroksidene som natriumhydroksid og kaliumhydroksyd. Cesiumhydroksid er faktisk etsende nok til å oppløses raskt gjennom glass. |  |
| Cesiumjodid: Cesiumjodid eller cesiumjodid er den ioniske forbindelsen mellom cesium og jod. Det brukes ofte som inngangsfosfor i et røntgenbildeforsterkningsrør som finnes i fluoroskopiutstyr. Cesiumjodid -fotokatoder er svært effektive ved ekstreme ultrafiolette bølgelengder. |  |
| Cesium litiumborat: Cesium litium borat eller cesium litium borate (CsLiB 6 O 10 ), også kjent som CLBO , er en ikke-lineær krystall for ultrafiolette applikasjoner og genererer den fjerde og femte harmoniske av Nd: YAG grunnleggende laserbølgelengde (1064 nm). | |
| Cesiumnitrat: Cesiumnitrat eller cesiumnitrat er et salt med den kjemiske formelen CsNO 3 . Et alkalimetallnitrat, det brukes i pyrotekniske sammensetninger, som fargestoff og oksydasjonsmiddel, f.eks. I lokkefugler og belysningsbluss. Cesiumutslippene skyldes hovedsakelig to kraftige spektrallinjer ved 852,133 nm og 894,347 nm. |  |
| Cesiumoksalat: Cesiumoksalat (standard IUPAC stave) dicesium oksalat, eller cesiumoksalat (amerikansk stave) er oksalatet av cesium. Cesiumoksalat har den kjemiske formelen Cs 2 C 2 O 4 . | |
| Cesiumoksid: Cesiumoksid (IUPAC -navn) eller cesiumoksid beskriver uorganiske forbindelser sammensatt av cesium og oksygen. Følgende binære (inneholder bare Cs og O) oksider av cesium er kjent: Cs 11 O 3 , Cs 4 O, Cs 7 O og Cs 2 O. Både oksydet og suboksidene er fargerike. Cesiumoksid refererer generelt til Cs2O, som er det enkleste og vanligste oksidet. Den danner gul-oransje sekskantede krystaller. |  |
| Cesiumperklorat: Cesium perklorat eller cesium perklorat (CsClO 4 ), er et perklorat av cesium. Det danner hvite krystaller, som er lite løselig i kaldt vann og etanol. Det oppløses lettere i varmt vann. | 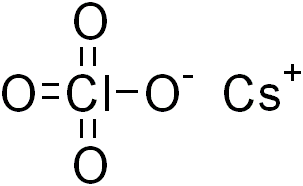 |
| Perkloratoborat: Perkloratoborat er en anion av formen [B (ClO 4 ) 4 ] - . Det kan danne delvis stabile faste salter med tunge alkalimetaller. De er mer stabile enn nitratoboratsalter. K [B (ClO 4 ) 4 ] brytes ned ved 35 ° C, Rb [B (ClO 4 ) 4 ] er stabil til 50 ° C, og Cs [B (ClO 4 ) 4 ] kan eksistere opptil 80 ° C. | |
| Cesiumstandard: Cesiumstandarden er en primærfrekvensstandard der fotonabsorpsjonen ved overganger mellom de to hyperfine jordtilstandene til cesium-133 atomer brukes til å kontrollere utgangsfrekvensen. Den første cesiumklokken ble bygget av Louis Essen i 1955 ved National Physical Laboratory i Storbritannia. og promotert over hele verden av Gernot MR Winkler fra United States Naval Observatory. |  |
| Cesiumsulfat: Cesiumsulfat eller cesiumsulfat er den uorganiske forbindelsen og saltet med formelen Cs 2 SO 4 . Det er et hvitt, vannløselig fast stoff som brukes til å fremstille tette vandige løsninger for bruk i isopyknisk (eller "tetthetsgradient") sentrifugering. Den er isostrukturell med kaliumsalt. |  |
| Cesiumsulfid: Cesiumsulfid (også stavet cesiumsulfid på amerikansk engelsk) er et uorganisk salt med en kjemisk formel Cs 2 S. Det er en sterk alkali i vandig løsning. I luften avgir cesiumsulfid råtten luktende hydrogensulfid. |  |
| Cesium titanat: Cesium titanat eller cesium titanat er en uorganisk forbindelse med formel Cs to TiO 3. Som de fleste andre uorganiske titanater, vedtar den en polymer struktur med Cs-O og Ti-O bindinger. | |
| Cesium tungstat: Cesium wolfram eller cesium wolfram er en uorganisk kjemisk forbindelse som er kjent for å danne en veldig tett væske i oppløsning. Løsningen brukes i diamantbehandling, siden diamant synker i den, mens de fleste andre bergarter flyter. | |
| Caesius: Caesius , blågrå på latin, kan referere til:
| |
| Caesius: Caesius , blågrå på latin, kan referere til:
| |
| Caesia -gener: Gens Caesia var en mindre plebeisk familie i det gamle Roma under den sene republikken, og gjennom til keiserlige tider. Det første medlemmet av denne generasjonen som oppnådde fremtredelse var Marcus Caesius, praetor i 75 f.Kr. Under imperiet ble Caesii utmerket for sine litterære prestasjoner. |  |
| Caesius Bassus: Gaius Caesius Bassus var en romersk lyrisk poet som levde i Neros regjeringstid. | |
| Caesius Nasica: Caesius Nasica var en romersk militæroffiser for den romerske keiserlige hæren. | |
| Kaeso: Kaeso kan referere til:
| |
| Caeso (praenomen): Caeso eller Kaeso er et latinsk praenomen , eller personlig navn, vanligvis forkortet K. Selv om det aldri var et vanlig navn, ble Caeso regelmessig brukt av en rekke fremtredende familier, både patricier og plebeier, i perioden i den romerske republikken. Den feminine formen er Caesula . Navnet ga også opphav til den patronymiske genen Caesonia. Kaeso er den eldre skrivemåten, som stammer fra perioden da bokstaven K fremdeles ble brukt ofte før vokalen A på latin, og før bokstavene C og G ble differensiert. | |
| Caeso Duillius: Caeso Duillius var en romersk politiker og medlem av Second Decemvirate i 450 og 449 f.Kr. | |
| Caeso Fabius Ambustus: Caeso Fabius Ambustus var en fire ganger konsulær tribune i Den romerske republikk rundt begynnelsen av 500- og 400-tallet f.Kr. | |
| Caeso Fabius Vibulanus: Caeso Fabius Vibulanus kan referere til:
| |
| Caeso Fabius Vibulanus (konsul): Caeso Fabius Vibulanus var konsul for den romerske republikken i 484, 481 og 479 f.Kr. Han hadde tidligere hatt kontoret til quaestor parricidii i 485 f.Kr. i forbindelse med rettssaken og henrettelsen av Spurius Cassius Viscellinus. | |
| Caeso Fabius Vibulanus (konsul): Caeso Fabius Vibulanus var konsul for den romerske republikken i 484, 481 og 479 f.Kr. Han hadde tidligere hatt kontoret til quaestor parricidii i 485 f.Kr. i forbindelse med rettssaken og henrettelsen av Spurius Cassius Viscellinus. | |
| Caeso Fabius Vibulanus: Caeso Fabius Vibulanus kan referere til:
| |
| Caeso Quinctius: Caeso Quinctius L. f. L. n. Cincinnatus var sønn av den romerske diktatoren Lucius Quinctius Cincinnatus. Hans rettssak for å hindre plebenes tribuner i 461 f.Kr. var en av de viktigste hendelsene i ordenenes konflikt i årene som ledet fram til decemviratet. | |
| Caeso Quinctius: Caeso Quinctius L. f. L. n. Cincinnatus var sønn av den romerske diktatoren Lucius Quinctius Cincinnatus. Hans rettssak for å hindre plebenes tribuner i 461 f.Kr. var en av de viktigste hendelsene i ordenenes konflikt i årene som ledet fram til decemviratet. | |
| Milonia Caesonia: Milonia Caesonia var romersk keiserinne som den fjerde og siste kona til keiseren Caligula fra ekteskapet i 39 e.Kr. til de begge ble myrdet i 41 e.Kr. |  |
| Caesonia -gener: Gens Caesonia var en plebeisk familie i det gamle Roma. De dukker først opp i historien under den sene republikken, og forblir i periferien til det romerske aristokratiet til Nero. En annen familie av Caesonii oppnådde konsulatet flere ganger fra slutten av det andre århundre; det er ikke klart hvordan eller om de var relatert til den tidligere Caesonii. | |
| Caesonius Bassus: Caesonius Bassus var en politiker fra det sene romerriket. Sannsynligvis sønn av Lucius Caesonius Ovinius Manlius Rufinianus Bassus, han var konsul for 317 sammen med Ovinius Gallicanus. Egyptiske kilder oppgir at de hadde sitt verv fra 8. januar, men kilder fra det vestlige Romerriket opplyser at de først kom til kontoret 17. februar. | |
| Blåmunnskinn: Den blåmunnede skinken er et skinn i. Det er monotypisk i slekten Caesoris . Det er endemisk for Ny -Caledonia. | |
| Blåmunnskinn: Den blåmunnede skinken er et skinn i. Det er monotypisk i slekten Caesoris . Det er endemisk for Ny -Caledonia. | |
| Caesorix: Caesorix var en leder av Cimbri-stammen under Cimbrian-krigen, der Cimbri vant en spektakulær seier mot romerne i slaget ved Arausio i 105 f.Kr. Han ble tatt til fange sammen med Claodicus i slaget ved Vercellae i 101 f.Kr. De andre kimbriske sjefene Boiorix og Lugius ble drept på feltet. | |
| Ordliste over botaniske termer: Denne ordlisten over botaniske termer er en liste over definisjoner av begreper og begreper som er relevante for botanikk og planter generelt. Vilkår for plantemorfologi er inkludert her, så vel som i den mer spesifikke ordlisten for plantemorfologi og ordliste for bladmorfologi. For andre relaterte termer, se Ordliste for fytopatologi og Liste over latinske og greske ord som vanligvis brukes i systematiske navn. | |
| Caespitotheca: Caespitotheca er en slekt av sopp i familien Erysiphaceae. Dette er en monotypisk slekt, som inneholder den enkelte arten Caespitotheca forestalis . | |
| Caespitotheca: Caespitotheca er en slekt av sopp i familien Erysiphaceae. Dette er en monotypisk slekt, som inneholder den enkelte arten Caespitotheca forestalis . | |
| Iain De Caestecker: Iain De Caestecker , er en skotsk skuespiller. Han er kjent for sine roller i filmene Shell (2012), In Fear (2013), Not Another Happy Ending (2013), Lost River (2014) og Overlord (2018). Fra 2013 til 2020 portretterte han Leo Fitz i TV -serien Agents of SHIELD |  |
| Stedsnavn opprinnelse: I store deler av den "gamle verden" kan navnene på mange steder ikke lett tolkes eller forstås; de formidler ingen tilsynelatende betydning i det moderne språket i området. Dette skyldes et generelt sett med prosesser der stedsnavn utvikler seg over tid, til deres åpenbare betydning går tapt. I kontrast til den "nye verden" er mange stedsnavn opprinnelse kjent. | |
| Mount Saint Peter: Mount Peter , også referert til som Caestert Plateau , er den nordlige delen av et platå som går nord til sør mellom dalene ved elven Geer i vest og Meuse i øst. Den går fra Maastricht i Nederland, gjennom Riemst i belgiske Limburg nesten til byen Liège i Belgia, og definerer dermed topografien til dette grenseområdet mellom Flandern, Wallonia og Nederland. Navnet på åsen, så vel som landsbyen og kirken Sint Pieter i nærheten og festningen Sint Pieter, refererer til Saint Peter, en av de tolv apostlene. |  |
| Caestocorbula: Caestocorbula er en utdødd slekt med saltvannsmuslinger i familien Corbulidae. Navnet er opprettet for fossiler fra eocene i Belgia. | |
| Caestocorbula: Caestocorbula er en utdødd slekt med saltvannsmuslinger i familien Corbulidae. Navnet er opprettet for fossiler fra eocene i Belgia. | |
| Caestocorbula: Caestocorbula er en utdødd slekt med saltvannsmuslinger i familien Corbulidae. Navnet er opprettet for fossiler fra eocene i Belgia. | |
| Caestocorbula: Caestocorbula er en utdødd slekt med saltvannsmuslinger i familien Corbulidae. Navnet er opprettet for fossiler fra eocene i Belgia. | |
| Caestocorbula: Caestocorbula er en utdødd slekt med saltvannsmuslinger i familien Corbulidae. Navnet er opprettet for fossiler fra eocene i Belgia. | |
| Caestocorbula: Caestocorbula er en utdødd slekt med saltvannsmuslinger i familien Corbulidae. Navnet er opprettet for fossiler fra eocene i Belgia. | |
| Caestocorbula: Caestocorbula er en utdødd slekt med saltvannsmuslinger i familien Corbulidae. Navnet er opprettet for fossiler fra eocene i Belgia. | |
| Caëstre: Caëstre er en kommune i Nord -avdelingen i Nord -Frankrike. |  |
| Cestus: En cestus eller caestus er en gammel kamphanske, noen ganger brukt i pankration. De ble slitt som moderne boksehansker, men ble laget med skinnstrimler og noen ganger fylt med jernplater eller utstyrt med kniver eller pigger, og brukt som våpen. |  |
| Caesulena gens: Gens Caesulena var en romersk familie under den sene republikken. Det er mest kjent fra taleren Lucius Caesulenus, som Cicero beskriver som en vulgær mann, dyktig til å trekke mistanke til personer og til å gjøre dem til kriminelle. Han var allerede en gammel mann da Cicero hørte ham. | |
| Caesulena gens: Gens Caesulena var en romersk familie under den sene republikken. Det er mest kjent fra taleren Lucius Caesulenus, som Cicero beskriver som en vulgær mann, dyktig til å trekke mistanke til personer og til å gjøre dem til kriminelle. Han var allerede en gammel mann da Cicero hørte ham. |
Thứ Sáu, 20 tháng 8, 2021
Isotopes of caesium
Đăng ký:
Đăng Nhận xét (Atom)
-
All Saints katolske skole, Dagenham: All Saints Catholic School er en romersk-katolsk ungdomsskole som ligger på Terling Road, Dagenha...
-
Romersk-katolske bispedømme av bregner: Stift av bregner er et romersk-katolsk bispedømme i det sørøstlige Irland. Det er en av tre su...
-
Bailar (sang): " Bailar " er en singel av meksikansk-amerikanske DJ Deorro med vokalen til Elvis Crespo. Bailar: Bailar ka...
Không có nhận xét nào:
Đăng nhận xét